アンモニア 混成 軌道 - 「sp3混成軌道,アンモニア」に関するQ&A
【文系女子が教える化学】混成軌道はなぜ起こる?混成軌道の基本まとめ
しかし、これは正しくないです。
異なる元素の混成軌道 メタンCH4、アンモニアNH3、水H2OのC、N、O はすべてsp3混成軌道で、正四面体構造です。
かがくののおと
そこで、スライド 13 の「本当はどうなっているのか」という話が登場するのです。
つまりメチルカチオンの腕は3本となり、 sp2混成軌道となります。
s軌道・p軌道と混成軌道の見分け方:sp3、sp2、spの電子軌道の概念
ただ全体的に考えれば、水素原子にある電子はK殻に存在する確率が高いというわけです。
s軌道は1つだけ存在しますが、p軌道は3つ存在します。
N原子のsp3混成軌道について教えてください.
sp2混成軌道:エチレン(エテン)やアセトアルデヒドの結合角 一方でsp2混成軌道はどのように考えればいいのでしょうか。
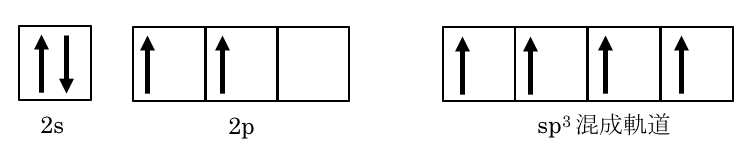
炭素は2s軌道に2個、2p軌道に2個の電子を有しており、不対電子を2個有している。
質問箱
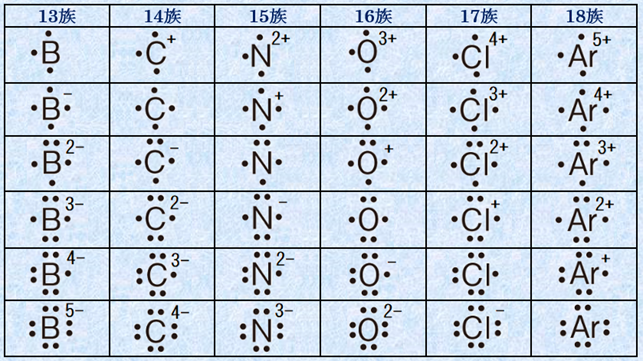
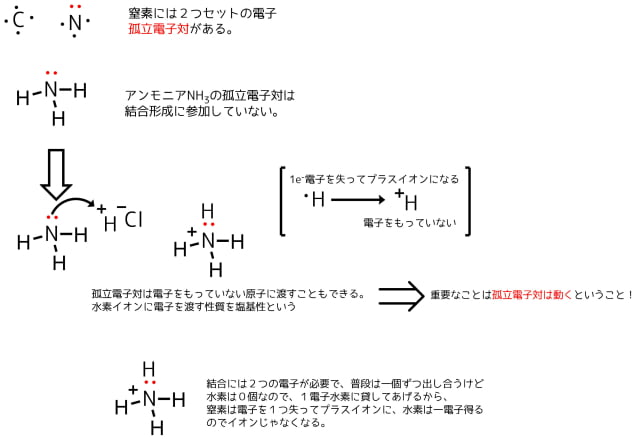
p軌道だけでは共有結合が作れない ここで、アンモニアの窒素Nの電子配置について考えます。
Hofmann ホフマン 転移のゴロを載せました。
【文系女子が教える化学】混成軌道はなぜ起こる?混成軌道の基本まとめ
このように、「 四つの手をもつ場合はsp 3混成軌道」と考えれば良い。
ボランのように二重結合がないものの、手が3本しかなく、sp2混成軌道になっている例外はあります。
「sp3混成軌道,アンモニア」に関するQ&A
アンモニアの構造は sp 3 混成のものだけ存在するのですか。
ただ深く考えても意味がないため、アンモニアや水は非共有電子対を含めてsp3混成軌道と理解すればいいです。
質問箱
Friedel-Crafts フリーデルクラフツ 反応アルキル化やアシル化を用いることで、ベンゼン環にアルキル基やアシル基などの炭素鎖を導入することが可能となります。
より詳しい混成軌道 手の数によって混成軌道を見分ける話をしたが、本当は「分子がどのような形をしているか」によって混成軌道が決まる。
- 関連記事
2021 www.dfe.millenium.inf.br