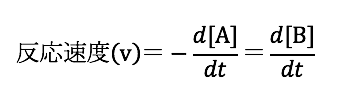反応 速度 単位 - 反応の速さと反応速度の求め方
反応次数と速度定数
ここで、 R は気体定数、 E a は活性化エネルギー、 T は系の温度、 C は頻度因子の定数です。
1 のようにグラフを作るのが困難な場合、濃度の時間微分によって、反応速度を求めることができません。
反応速度と化学平衡
反応速度 反応速度とは、 単位時間あたりの反応物(あるいは生成物)の濃度変化のことをいいます。
ル・シャトリエの法則 化学反応は、生成物のエンタルピー H が小さく、生成物のエントロピー S が大きいほど、その状態が実現しやすいということになります。
反応速度式とは?計算方法や求め方のなぜをわかりやすくグラフで解説!温度/濃度/係数/単位の覚え方【高校化学】
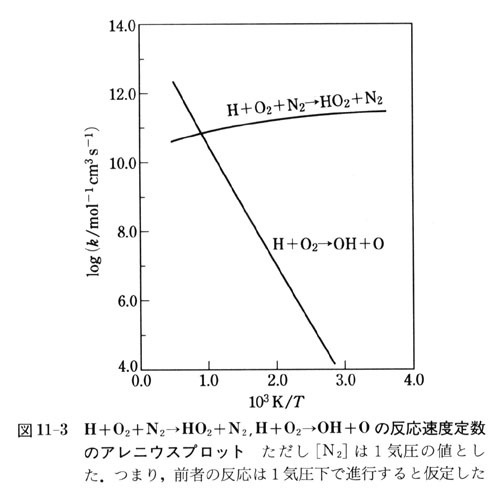
反応速度定数 k と温度 T は、実験により測定可能な値なので、このグラフより、傾きを求めることができます。
には火薬ののようにきわめて速い反応、水溶液中での金属イオンの沈殿反応のような速い反応から、デンプンの加水分解反応、湿った空気中での鉄片が錆びる反応などのようにゆっくりとした反応がある。
第106章 反応の速さ
出典 ブリタニカ国際大百科事典 小項目事典 ブリタニカ国際大百科事典 小項目事典について 「反応速度」の解説. そのため、反応時間のどのタイミングで接線の傾きを求めるかによって、接線の傾きは変化してしまいます。
しかし、反応物同士が衝突したからといって、必ず反応するとは限りません。
反応次数と速度定数
(活性化エネルギーについては「」の記事で詳しく解説しているので是非参考にしてください。
塩化ナトリウムNaCl水溶液に硝酸銀AgNO 3水溶液を加えると,ただちに塩化銀AgClの白色沈殿が生じますね。
反応の速さと反応速度の求め方
触媒は、反応物との間で、反応中間体を作ります。
粒子が移動しやすい気体や溶液中の反応では、反応物の濃度を大きくすると、反応物同士が衝突する確率が大きくなるので、反応速度は大きくなります。
- 関連記事
2021 www.dfe.millenium.inf.br