金属 イオン化 傾向 覚え 方 - ぼくの高校レベルのイオン化傾向の覚え方
イオン化傾向と反応性の覚え方|歌/大きい順/中学/高校
かくいう私も暗記が苦手なこともあって理系にしたのに、「化学の時間はよくわからない言葉をたくさん覚えなくちゃいけない」と大変憂鬱に思っていたことがあります。
なぜかというと、 まず同族元素の場合、が大きいと電子殻の枚数が多くなります。
イオン化傾向と電池~理論化学超特急丸わかり講座⑪
それがコチラ。
このとき、傷がついた部分に雨水が付着すると、水中に溶けている酸素が金属から電子を奪おうとします。
イオン化 傾向 ゴロ
最近、突然話しかけられたこと。
コツコツと演習した努力の積み重ねが、そのまま点数に還元される分野なので、積極的に問題演習をしてください。
イオン化傾向とは?覚え方も使い方もこれでバッチリ!|高校生向け受験応援メディア「受験のミカタ」
理論的に説明できないイオン化傾向は覚えるしかありませんよ。
の小さいスズが鉄を守るので錆びにくく、美観を保ちます。
金属 イオン化 傾向 覚え 方
最後に使い方をご紹介します。
水素は金属ではありませんが陽イオンになる基準として入れておきましょう。
イオン化傾向(イオン化列)と反応性 金属の酸化還元
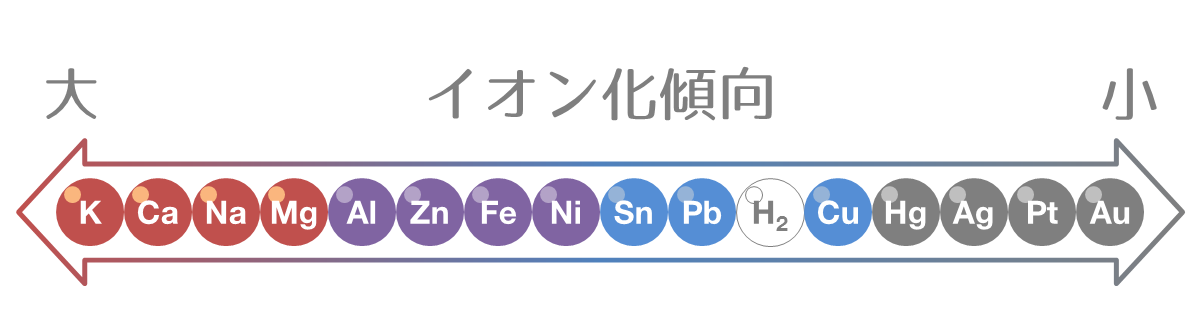
(リチウムやベリリウムなどは、高校受験のレベルではほとんど使用されません) 実際に大学受験の入試問題で使用される水素を含む物質は、イオン化傾向の大きい順に、リチウム、カリウム、カルシウム、ナトリウム、マグネシウム、アルミニウム、亜鉛、 鉄、ニッケル、鈴、鉛、水素、銅、水銀、銀、プラチナ、金と、高校受験の場合と比較すると桁違いに数が多いです。
イオン化傾向と金属の反応性 イオン化傾向と金属の反応性には関連があります。
【化学基礎】イオン化傾向とは何なのかを徹底解説!語呂合わせと使い方もご紹介
電子が外れやすい順に金属イオンを並べたもの、という風に、の定義は言い換えることができます。
水素よりイオン化傾向が大きければ水素は発生するけど、水素よりイオン化傾向が小さければ水素は発生しません。
- 関連記事
2021 www.dfe.millenium.inf.br