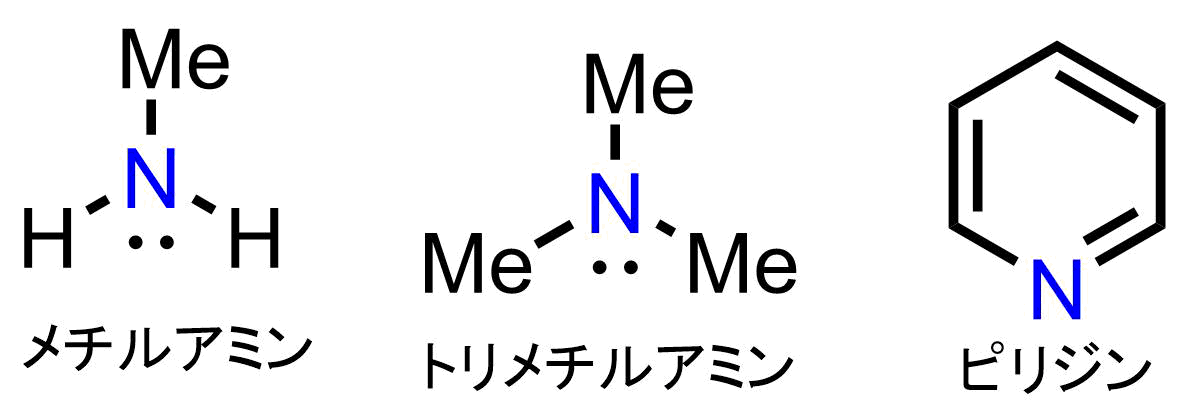窒素 電子 式 - 窒素(N2)の化学式・分子式・構造式・電子式・分子量は?窒素の代表的な反応式は?
分子と共有結合
原子の電子式一覧 原子番号1〜18の原子の電子式を一覧にまとめておきます。
亜硝酸塩は安定で種々の塩が知られている。
窒素(N2)の化学式・分子式・構造式・電子式・分子量は?窒素の代表的な反応式は?
35)、不安定なため単離できず水溶液中でも徐々に分解する。
そしてそれはBのレベルへと緩和する。
⑦酸化還元反応:電子のやり取り
「太陽系探検ガイド エクストリームな50の場所」p140 デイヴィッド・ベイカー、トッド・ラトクリフ著 渡部潤一監訳 後藤真理子訳 朝倉書店 2012年10月10日初版第1刷• 水溶性• 拡散や衝突によって失われる時間というのは、これよりもずっとずっと短い時間じゃ。
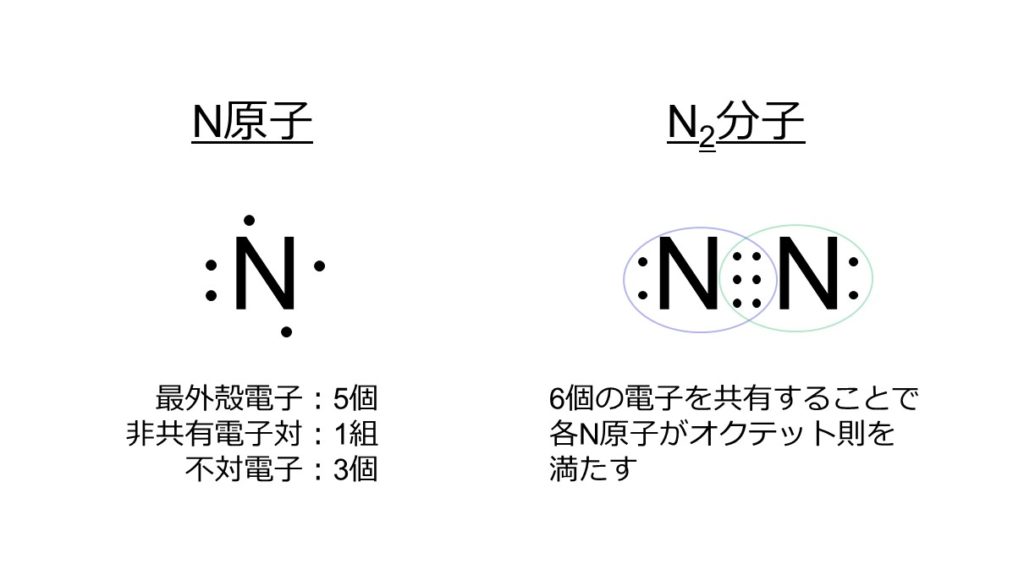
簡単に説明 第2周期の原子の最外電子殻 L殻 には、最大で電子が8個入る ただ、電子配置図のように電子が円形に並ぶわけではなく、電子が2個ずつ入ることのできる部屋が4つあり、そこに電子が収容されていくことになる この電子の、部屋への入り方にも規則があり、一部に偏ることがないように、できるだけ均等に入っていく L殻に電子が2つ入る時、2つまとまって電子対となって1つの部屋へ入るのではなく、1個ずつ2つの部屋へ入るの 窒素の場合、L殻に入る電子は5つ 5つを4つの部屋にできるだけ均等に振り分けると、 2,1,1,1 となる 電子対が1組でき、不対電子が3つできる 分子を形成するとき、電子が余ることがないように共有結合を形成する なので窒素は不対電子3つを他の窒素と共有し三重結合となる. 次は準安定状態について見てみよう。
窒素分子の発光スペクトル|アリオス株式会社
例えば、第1族の水素原子 H:2. しかし、最外殻電子は8個でありオクテットで他の原子とは反応しないため、0個となります。
お互いに電子を3個ずつ出し合うことによって、 N原子2つで計6個の電子を共有します。
【図解】最外殻電子と価電子の定義と違い⇒結論:希ガスでことなります
最外殻はL殻で、最外殻電子は5個です。
そもそも、共有結合は何のためにするのか考えると良いです。
窒素の電子式はなぜ・・・・N:N・・・・にはならず:N:::N:(3重結...
実際の分子は、それぞれ固有の形をしている。
これで解決!シリーズ 大学物理 窒素分子スペクトルの巻 公開中の授業 原子分子エネルギー 偏微分の基礎 窒素分子スペクトル 水素やヘリウムスペクトルなどの簡単なスペクトルはかなり突っ込んで学習したね。
元素の周期表・電子配置
まず、下に示したエネルギー図を見てみよう。
窒素の解離が分光的には観測できないことを意味していると考えた方が良さそうです。
なぜ窒素N2は三重結合なんですか? 写真のように単結合はできないんですか?
もちろんこの第一正帯の遷移は幅が広いから、赤色に光る遷移もあるぞ。
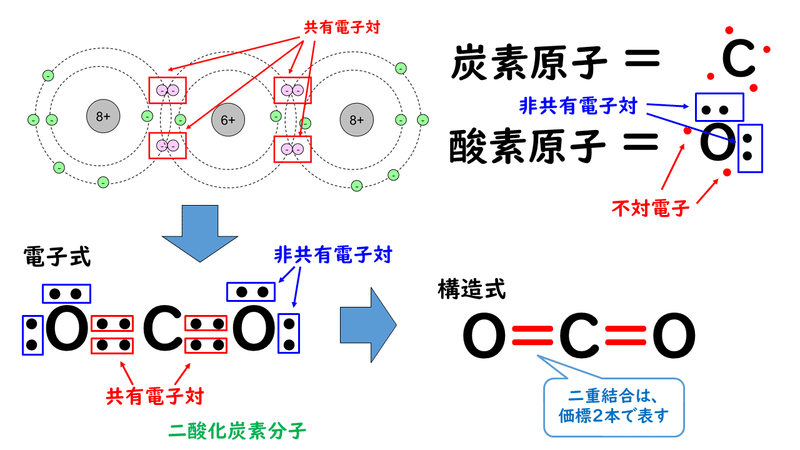
1.分子 物質を構成する粒子の1つに、いくつかの原子が結びついてできた分子がある。
- 関連記事
2021 www.dfe.millenium.inf.br